巴西医美脱毛设备注册全攻略:市场为什么火爆?注册到底有多保守?如何合规切入?

巴西是全球第二大美容手术大国,医美激光市场体量巨大,但脱毛设备(激光脱毛/ depilação a laser)的ANVISA注册却非常低调,真正明确写 “脱毛适应症” 的产品凤毛麟角,大多数厂商都选择用更宽泛的描述,如 “Sistema de laser para terapia” 或 “dermatological laser” 来规避风险。
今天我基于真实ANVISA数据库、市场报告和注册实际经验,系统分析为什么巴西脱毛设备好卖、为什么不直接写 “脱毛” 、注册的风险点和独特之处,最后附上已注册产品的巴西经销商名单,可直接开发。
一、为什么脱毛设备在巴西特别好卖?(市场需求分析)
巴西激光脱毛市场保持高速增长,2022年规模约5030万美元,2024年已增长至约 7630万美元,2025年达到9500万美元,复合年增长率(CAGR)稳定在23%左右,预计2030-2035年将突破数亿美元,成为拉美最具爆发力的细分赛道之一。
核心驱动因素有4个:
- 强悍的美容文化和热带气候
随着巴西中产群体不断壮大,可支配收入持续提升,越来越多消费者愿意为专业激光脱毛设备和服务买单。他们追求 “一次投资、多疗程近乎永久” 的高效解决方案。相比传统的剃须、蜜蜡脱毛或家用产品,激光脱毛具有安全系数高、治疗快速、恢复期短、效果持久等显著优势,完美匹配现代都市人 “高效美容、轻医美” 的消费偏好。
二、巴西这类产品以什么类别注册?风险等级如何?
根据ANVISA现行法规RDC 751/2022,医美激光/光脱毛设备属于医疗设备(Equipamentos Médicos),明确涵盖了美容与美学用途(embelzamento e estética)。
风险分类(Classificação de Risco):
根据Annex I 的22条分类规则,脱毛设备分类主要取决于技术类型和能量强度:
1. 高能量二极管激光、Nd:YAG等有源激光系统,通常判定为Class III类高风险,属于主动式治疗设备,能量高、穿透深,需严格控制安全性和有效性。
2、IPL强脉冲光、LED光脱毛系统则多为Class II类中风险。
注册路径:
1. Class III需要走Registro路径,即完整注册,需要ANVISA技术审查,证书有效期10年,可续期。
2. Class II则只需走Notificação路径,即简化通知,证书无固定有效期,注册流程十分快,能更快进入市场。
三、为什么有的产品明确写 “脱毛”(depilação),有的却选择不写?
从ANVISA最新数据库可以看到,大量产品直接使用了脱毛depilação 或 激光脱毛depilação a laser等明确表述,同时也有不少产品采用激光治疗系统Sistema de Laser para Terapia 或 皮肤治疗系统Sistema Dermatológico等宽泛名称。
1. 单一适应症 vs 多用途平台
路径一:明确写脱毛depilação适用于专用脱毛设备或商业定位清晰的医美脱毛产品。 其特点是适应症明确,技术文件和临床证据需要直接对应“脱毛效果”,ANVISA审评时会更聚焦于能量参数、安全性以及针对不同肤色的疗效数据。这种写法优势在于市场推广时卖点突出,但审评资料要求相对更高。
路径二:采用宽泛描述的平台型设备常见表述为皮肤治疗系统或激光治疗系统。 这类写法更适合多功能激光平台,同时支持脱毛、嫩肤、血管治疗等多种用途。它能避免被单一适应症锁死,便于未来拓展新用途,技术文件也更侧重通用性能和整体安全性,审评相对灵活。
2. 全生命周期管理
3. 关于标签外使用(off-label)
在巴西医疗实践中,医生确实拥有一定的临床裁量权(clinical discretion),可在合规前提下根据专业判断使用设备。但必须注意,注册适应症仍是监管核心依据。off-label使用不属于监管鼓励的方向,从合规角度看,它从来不是一个可以依赖的注册方案,一旦发生不良事件,责任风险会显著增加。因此,我们在注册阶段仍应优先制定清晰、可充分支撑的适应症方案,而非依赖off-label空间。
四、脱毛设备巴西注册的风险、独特点详解
1. 注册路径的核心优化:AREE依赖路径(Regulatory Reliance)
- Class II类设备,如IPL、LED脱毛仪,走通知路径(Notificação),审核很松,材料完整的情况下通常1–2个月即可取证。
- Class III 类设备,如高能量激光、二极管激光、Nd:YAG,必须走注册路径(Registro),传统审评周期约12–18个月。
近年来,ANVISA逐步引入基于等同监管机构(AREE)的依赖审评机制。如果产品已获得美国FDA的510(k)、加拿大Health Canada的MDL、澳洲TGA全面审核或日本PMDA的实质性批准,且技术文件、制造信息完全一致,可在部分项目中提升审评效率,Class III 案例可压缩至4–8个月。但需注意,ANVISA仍保留完整技术审查权,它不是一个可以直接放行的快速通道,而是在同等条件下更容易被优先审评。
2. BGMP 与 MDSAP
Class II类设备虽然必须遵守巴西BGMP质量管理体系要求,无需提交BGMP证书,但仍需证明其质量体系符合ANVISA要求,通常通过ISO 13485的方式体现,不需要接受ANVISA的现场审计,合规门槛较低。
Class III 类设备则必须符合巴西BGMP(Brazil Good Manufacturing Practices)要求。ANVISA高度认可MDSAP(Medical Device Single Audit Program)证书,可将其作为BGMP的重要审查依据,并显著减少或豁免现场检查的频率和范围。但这并不等同于完全免除BGMP审查,我们仍需做好充分的技术文件和质量体系准备,以顺利通过ANVISA的最终审核。
3. INMETRO认证:有源设备强制要求
所有带能源的有源医疗设备(包括激光设备)必须通过INMETRO强制性合格评定,获得认证标志后方可合法销售。中国厂家常见问题在于IEC 60601标准版本不匹配或测试报告需补充本地认可实验室数据。
典型周期:完整INMETRO认证通常需要6-9个月,包括实验室测试(IEC 60601系列等)、质量体系审核(ISO 13485相关)及工厂评估。

这个也是ANVISA重点审查的内容,需严格按照要求设计并翻译成葡语,不能仅使用英文。Class 4激光警示标签核心要素包括:
- 信号词:DANGER(危险),红色背景或醒目字体
- 激光辐射警示符号:三角形内有激光束图标
- 主要警告语句:
-
“LASER RADIATION – AVOID EYE OR SKIN EXPOSURE TO DIRECT OR SCATTERED RADIATION” -
“CLASS 4 LASER PRODUCT” - 其他必填信息:
-
激光波长(例如 808 nm) -
输出功率(例如 Maximum Output: 50W) -
制造商名称和地址 -
生产日期或序列号 -
符合的标准(IEC 60825-1 或 FDA 等)
-
其他标签要求:
五、巴西医美设备的经销商名单(可直接开发)
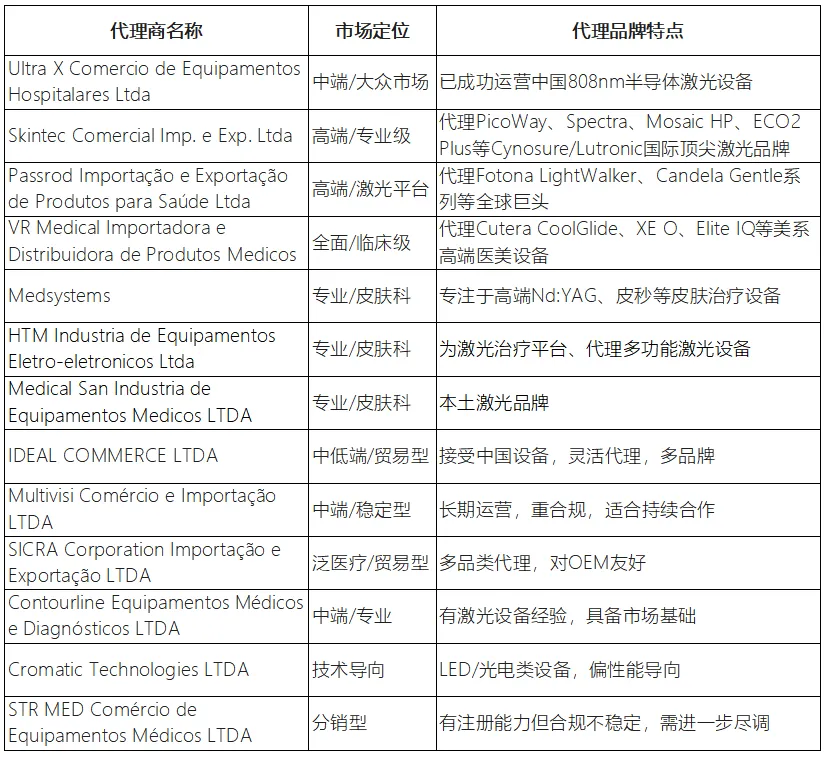
以上均为公开信息,如需具体联系方式(邮箱、电话、负责人)、合作切入方案、定制项目分析报告,随时留言或私聊我,我可以帮你精准对接或进一步核查和背调。