160亿美元AD市场,“新王炸”来袭
阿尔茨海默病(AD)药物市场正进入价值重构阶段。根据business research insights预测,全球AD药物市场规模将在2026年达到92.2亿美元,到2035年增至158.7亿美元,2026年至2035年的复合年增长率为6.23%。
过去,AD患者规模持续扩大,疾病负担不断累积,但临床可提供的药物大多停留在症状改善层面,市场空间并没有真正释放。近两年,随着Aβ单抗相继上市,疾病修饰治疗开始进入真实世界,AD药物市场才出现了更明确的变化。
这一轮市场升温背后,以礼来的Remternetug、罗氏的Trontinemab及TauRx的HMTM为代表的“新王炸”产品正蓄势待发,推动AD药物向给药更便利、脑穿透能力更强的方向迭代。
160亿美元的市场,开始从预期走向兑现。
01
160亿美元AD市场
AD是发生于老年和老年前期的中枢神经系统变性疾病,临床上以进行性认知功能障碍和行为损害为主要特征,患者会逐步出现记忆障碍、失语、失认、视空间能力下降,以及人格和行为改变。病理上,AD主要表现为脑内Aβ沉积形成的神经炎性斑和过度磷酸化Tau蛋白形成的神经原纤维缠结。
AD这一疾病的市场基础并不缺患者,而是缺少真正有效的新药供给。国际阿尔茨海默病协会2021年数据显示,全球痴呆患者已超过5500万人,预计2030年将达到7800万人。《中国阿尔茨海默病报告2024》显示,2021年我国现存AD及其他痴呆患病人数接近1700万,占全球总数近30%。
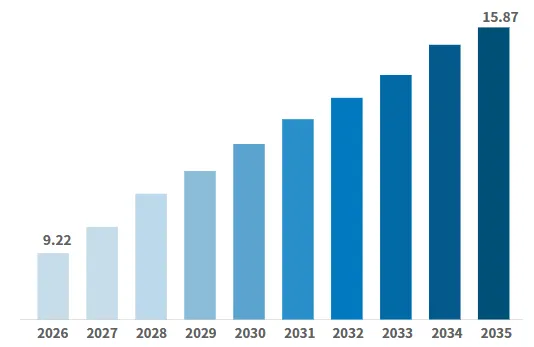
图1 2026-2035年AD药物市场规模(十亿美元)
图片来源:business research insights
据business research insights预计,全球AD市场规模将在2026年达到92.2亿美元,到2035年增至158.7亿美元,2026年至2035年复合年增长率为6.23%(图1)。AD的市场基础已经足够稳固,市场扩容更多取决于治疗手段是否真正升级。
从已上市药物看,AD治疗过去很长时间主要停留在对症阶段。多奈哌齐、卡巴拉汀、加兰他敏等胆碱酯酶抑制剂,适用于轻中度患者,通过提高乙酰胆碱水平改善认知功能;美金刚作为NMDA受体拮抗剂,主要用于中重度患者,作用机制是阻断异常谷氨酸信号导致的钙离子持续内流,减轻神经细胞损伤。临床前研究提示,美金刚还可降低Aβ水平,改善Aβ引起的LTP异常。除此之外,苏沃雷生、布瑞哌唑分别覆盖行为和情绪症状管理。也就是说,传统AD药物能够改善部分症状,但很难改变疾病进展,这也是该领域多年商业天花板不高的根本原因。
近两年,随着Aβ单抗相继上市,AD市场进入了一个新阶段。仑卡奈单抗和多奈单抗分别于2023年和2024年获FDA批准,用于治疗轻度认知障碍或阿尔茨海默病所致轻度痴呆患者,AD治疗的目标也由过去的症状改善,开始延伸至疾病进展延缓。此后,两款药物又分别于2024年1月5日和2024年12月17日获NMPA批准上市。商业化上,仑卡奈单抗已进入快速放量阶段,2025年销售额达到4.54亿元,较上年全年增长超过200%;多奈单抗由于上市时间较晚,目前销售仍处于低位。Aβ单抗获批后,早期AD患者的治疗选择被进一步打开,160亿美元AD市场开始醒来。
02
全球研发格局
进入在研阶段后,AD药物的研发重心已经比较集中,Aβ和Tau仍是最核心的两条主线。Aβ方向的项目数量最多,但成药难度并没有因为已有产品上市而明显下降。真正进入晚期临床后,淘汰率依然不低。
据东北证券研报,截至2025年11月,全球处于临床阶段的Aβ靶点药物共54项,其中处于III期阶段的有10款。这10款产品已有3款披露结果不佳,另有2款临床试验终止,Aβ仍然属于高投入、高失败率的难成药靶点。也正因为如此,这一赛道虽然热度高,竞争格局却谈不上拥挤到无缝可插,后发者仍有追赶空间。
此外,现阶段Aβ药物之间的竞争,已经不再只看斑块清除本身,给药便利性、长期安全性以及在早期患者中的持续获益,正变得越来越重要。
礼来的多奈单抗自2024年以来已被中国、美国、日本、英国、澳大利亚和EMA批准上市,仑卡奈单抗上市时间更早,获批国家更多。在这基础上,礼来又推进了Aβ清除率更高且采用皮下注射的Remternetug,希望继续强化产品竞争力。
Remternetug是一种抗淀粉样蛋白抗体,被定位为多奈单抗的继任者,目前正在1600余名早期有症状阿尔茨海默病患者中开展试验,同时评估皮下注射和静脉注射两种剂型,主要终点聚焦于淀粉样斑块清除效果。
2023年阿尔茨海默病和帕金森病国际会议(AD/PD 2023)发布的报告显示,Remternetug用以治疗轻度认知功能障碍或轻至中度AD患者的多中心、随机、双盲1期临床试验取得积极结果,中期分析结果显示Remternetug可快速且稳定地清除淀粉样斑块。目前,Remternetug已进入III期阶段,礼来预计于今年公布其3期TRAILRUNNER-ALZ 1研究顶线数据。
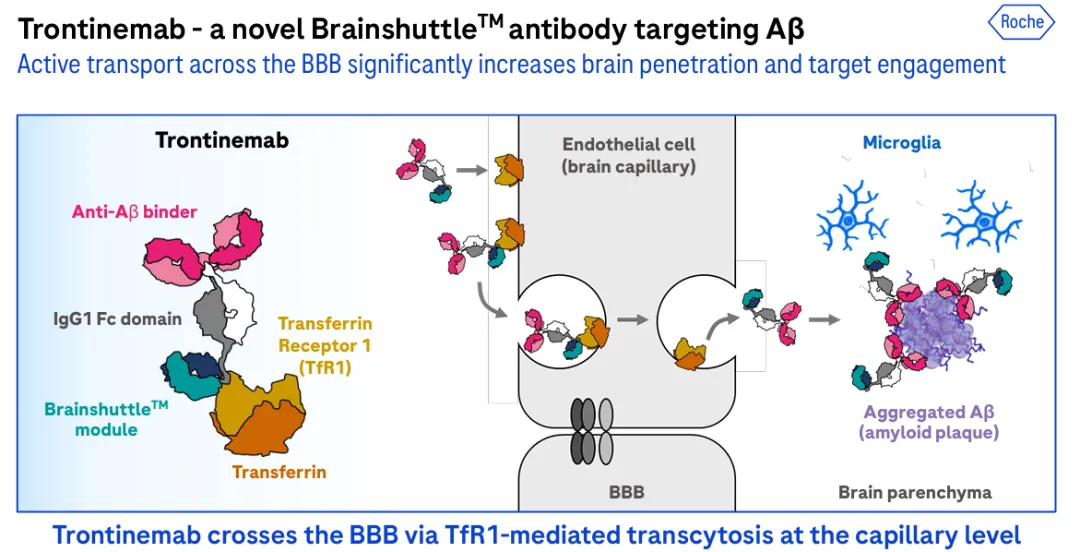
图2 Trontinemab作用机制
图片来源:罗氏官网
与此同时,罗氏布局的Aβ双抗管线Trontinemab也已推进至III期临床,Trontinemab是一款运用罗氏大脑穿梭(brain shuttle)技术的靶向淀粉样蛋白单抗(图2)。该药物将靶向淀粉样蛋白的单抗与能结合转铁蛋白受体的蛋白结构域融合,从而协助其穿越血脑屏障,在用药3-6个月后可以快速有效地清除大脑中的淀粉样蛋白沉积。
I/II期临床中,所有患者均实现Aβ减少,91%的患者达到完全清除,高剂量组平均降幅达-99 CL,相比之下,同类药物多奈单抗和阿杜卡单抗在TRAILBLAZER-ALZ 4试验中治疗6个月后平均降幅仅为-62 CL和-16 CL,实现清除的患者比例也远低于Trontinemab(38%和2%)。基于临床数据,罗氏于2025年启动两项III期临床试验,该药物已迈入上市前的关键阶段。
除礼来和罗氏外,Aβ赛道的技术竞争还在继续延伸。2024年10月,艾伯维以14亿美元现金收购Aliada,获得其血脑屏障穿透技术及核心管线ALIA-1758。ALIA-1758是一款3pE-Aβ抗体,可通过转铁蛋白受体介导穿透血脑屏障,实现β淀粉样蛋白斑块的降解与清除。
相较Aβ,Tau方向的研发推进得更慢。针对Tau蛋白异常假说,目前临床进展最快的是TauRx Pharmaceuticals研发的甲磺酸氢甲硫堇(HMTM,TRx0237),已进入III期临床,该药物主要靶向大脑内神经细胞所形成的Tau蛋白、TDP-43蛋白和突触核蛋白的异常聚集、错误折叠及其纤维缠结,是全球首个进入晚期临床的口服Tau聚集抑制剂。
从当前在研格局看,AD药物开发还没有真正收敛。Aβ已有上市药物和长期随访数据支撑,后续项目主要围绕更高效清除、更便捷给药方式和更稳定安全性继续迭代;Tau则刚开始进入晚期临床验证阶段。
03
中国力量崛起
近年来,国内企业已进入AD创新药开发序列,但整体仍处在跟跑阶段。
现阶段,国内在研管线中,推进速度相对靠前的是恒瑞医药的Aβ单抗SHR-1707(II期临床),其余多数项目仍停留在I期阶段。
SHR-1707是一种新型人源化抗AβIgG1单抗,能够特异性结合Aβ原纤维和单体,阻止Aβ斑块的形成并促进小胶质细胞对Aβ的吞噬清除,用于治疗AD。临床前5xFAD转基因小鼠模型数据显示,SHR-1707能够显著减少脑内Aβ沉积,且未见明显安全信号。2023年,恒瑞公布了该药在中国和澳大利亚开展的两项I期研究结果,完成了首次人体验证。目前,SHR-1707已进入II期临床,属于国内进度最快的Aβ在研管线。
除单抗外,国内企业也在尝试口服小分子路线。新华制药的OAB-14是一款多靶点口服小分子Aβ清除剂,来源于对2012年《Science》期刊报道的Aβ淀粉样蛋白清除化合物Bexarotene作用机制的进一步改造。现有研究显示,OAB-14能够明显减少脑内Aβ淀粉样蛋白沉积,降低Tau蛋白过度磷酸化,并改善APP/PS1双转基因AD模型小鼠的学习记忆障碍。该药已于2025年6月19日完成II期临床首例患者入组,拟用于轻中度AD,目前仍处于临床推进阶段。
恩华药业则把研发方向放在了神经炎症机制上。其子公司上海枢境生物自主研发的NH280105,是一款口服高选择性脂蛋白相关磷脂酶A2(Lp-PLA2)抑制剂,也是全球首款针对AD进入海外I期临床试验的Lp-PLA2靶点创新药,目前仍处于临床早期。
根据公司披露,Lp-PLA2是AD病理进程中的关键炎症调控靶点,异常激活会加剧神经损伤;NH280105通过抑制该靶点,试图实现抗炎、修复屏障、减少病理沉积并改善认知的连续作用。和Aβ单抗这类已有上市先例的项目相比,NH280105所处的赛道更早,临床转化的不确定性也更高,但它反映出国内企业对AD研发的布局已经不再局限于Aβ方向,开始向神经炎症等新机制延伸。
整体看,国内企业与MNC之间仍存在明显的研发进度差距,但现有项目思路并不雷同,且已从单一跟随转向机制分化。
04
结语
Aβ单抗的成功破冰,为阿尔茨海默病治疗打开了新局面。而后续围绕给药便利性、脑穿透效率及全新作用机制的持续迭代,将进一步推高这一赛道的天花板。
注:本文仅作信息交流之目的,文中观点不代表药智网立场,也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
参考资料
[1]https://www.businessresearchinsights.com/zh/market-reports/alzheimer-market-125374
[2]https://medically.roche.com/content/dam/pdmahub/restricted/neurology/ctad-2024/CTAD-2024-presentation-kulic-latest-interim-results-from-brainshuttle-ad-study.pdf
[3]https://assets.roche.com/f/176343/x/6d66b8d069/neurology-ir-event_adpd_04-apr2025-finalfinal_wo-speaker-notes.pdf
[4]东北证券研报,各企业官网等
责任编辑 | 史蒂文
合作、投稿、转载开白 | 马老师 18323856316(同微信)


 阅读原文,是受欢迎的文章哦
阅读原文,是受欢迎的文章哦