制氧机美国市场准入流程|便携制氧机-510(K)审核要点与检测要求成功案例全解


便携制氧机分类:Class II类
产品代码:CAW
认证路径:510(k)
GMP:非获免(上市后验厂)


510(K)文件编写的资料需要筹备的资料:
1)产品描述,含产品图片、图纸、预期用途、功能介绍、结构、组成、材料、工作原理等
2)标签样稿及说明书
3)包装描述及设计图
4)软件开发文档
5)风险分析(适用时)
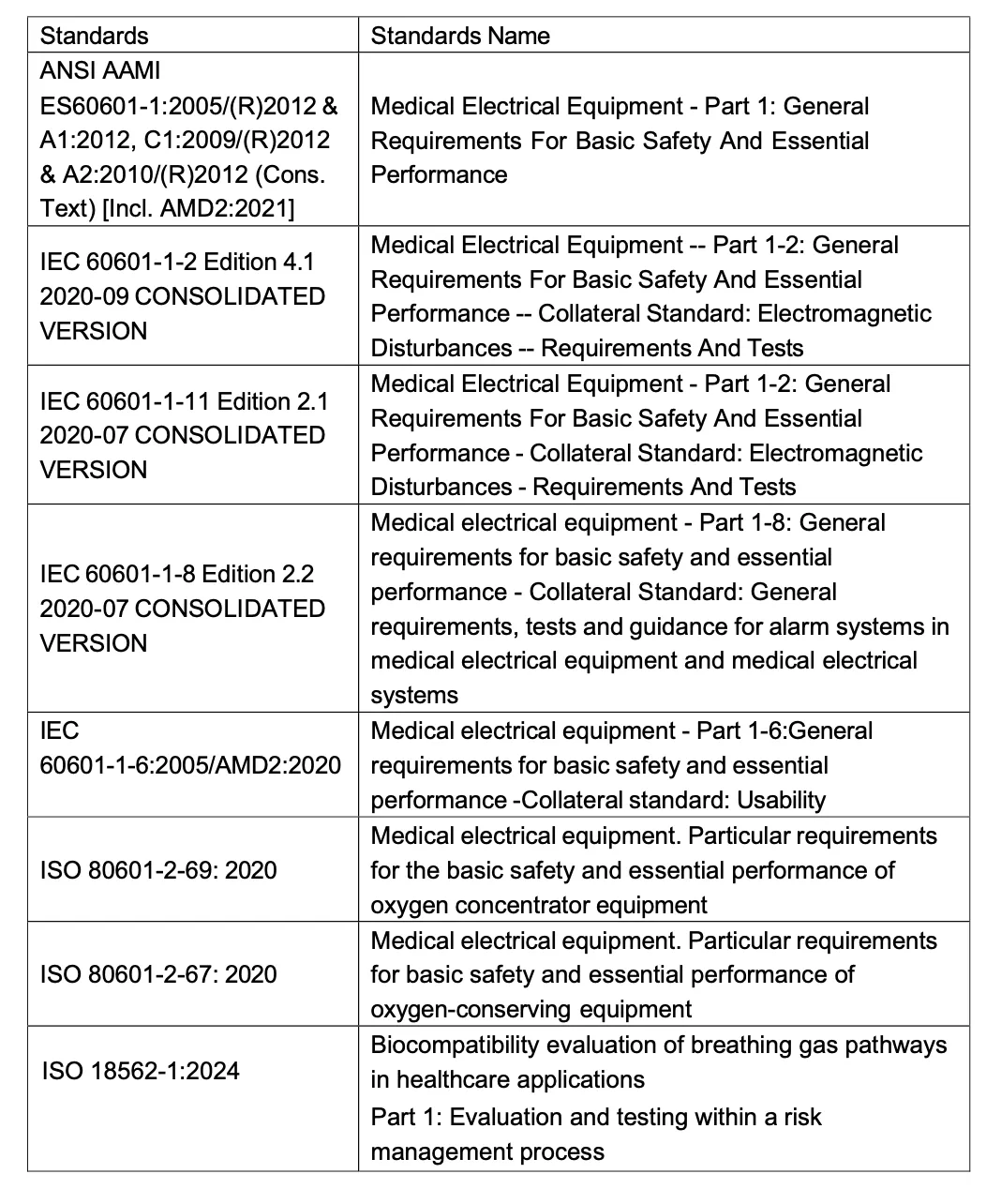
6)检测报告
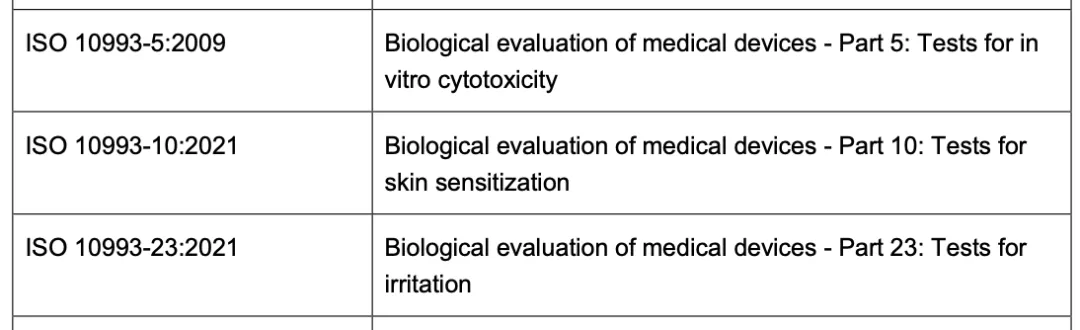
检测注意事项和难点:主要集中于ISO 10993和ISO 18562
在2024-2026年堪称中国生物学GLP实验室的“黑色星期五”众多的实验室被美国FDA列入实验室黑名单,那么我们的检测安排该何去何从,才不会在FDA审批的过程中被提出种种质疑或者直接判定为“假报告”,联系万易咨询为您提供海外实验室合规方案

呼吸类产品ISO18652检测全解析 & 万易咨询Winning专业服务
ISO18652是制氧机、呼吸机、雾化器、呼吸过滤器等呼吸气体相关设备及耗材的核心检测标准,该标准检测不仅FDA审批要求严苛,CE-MDR认证同样强制要求,是呼吸类医疗产品全球上市的关键准入门槛。
ISO18652核心检测特点
1. 严苛测试条件
测试需基于临床使用最差情况设计,遵循国际顶级实验室规范,质量体系、数据完整性、专业评估、全程可追溯均需达标;试验环境、流速、流量、使用时长均需与临床实际高度匹配。
2. 样品测试规范
可采用终产品、组件、试制样品开展测试,若使用试制样品,需明确与终产品差异,并提供不影响生物相容性的完整理论依据。
3. 颗粒物释放管控(ISO18562-2)
呼吸气路内表面必须做颗粒物释放评估,检测范围锁定0.5~10μm(肺部易沉积关键粒径);限值要求:≤2.5μm粒子≤12μg/m3,≤10μm粒子≤150μg/m3,测试方法包含过滤称重法与粒子计数法。
4. 有机挥发物(VOCs)释放管控
所有气体通道需评估VOCs排放量,检测范围为沸点50°C~260°C常规VOCs,限值按使用时长分级:短期接触(≤24h)≤360μg/d;长期接触(24h<使用时长<30天)≤120μg/d;永久接触(≥30天)≤40μg/d(制氧机被FDA归类为永久接触器械)。
5. 冷凝水析出物要求(ISO18562-4)
气路产生冷凝水的产品,需评估有害浸出物风险;仅患者可接触冷凝水的管路需测试,已通过ISO10993-1生物相容性评估的产品(如气管插管)可豁免。
FDA特殊认可要求
1. 呼吸机等有源呼吸器械,额外检测一氧化碳、二氧化碳、臭氧等无机气体;
2. 冷凝水可沥滤物分析,FDA不认可纯水提取,需按ISO10993-18增加半极性/非极性溶剂浸提研究。
认证痛点
不同实验室检测执行标准、报告内容差异极大,极易导致FDA审核出现大量发补问题,延误产品上市周期、增加成本投入,专业检测机构与咨询团队的配合至关重要。
万易咨询Winning · 认证咨询+呼吸类产品ISO18652检测一站式解决方案
万易咨询Winning深耕呼吸类医疗产品检测认证领域,为您提供全流程、专业化、落地性的ISO18652检测辅导,助力产品快速通过FDA、CE-MDR审核,少走弯路、节省时间与成本。
✅ 定制化检测方案:结合产品特性、临床场景与监管要求,量身打造合规检测方案
✅ 全程过程跟踪:把控测试全环节,确保样品、条件、数据符合标准要求
✅ 授权实验室对接:联动国际权威授权实验室,保障检测资质与结果认可度
✅ 检测报告审核:严格核查报告完整性、合规性,规避审核发补风险
✅ FDA发补整改:针对审核问题提供专业整改方案,快速通过终审
选择万易咨询Winning,让呼吸类产品市场准入更高效、更合规、更省心!
下一篇|呼吸机美国市场准入|睡眠呼吸机-510(K)审核要点与临床检测要求解析



评论