营销信息|疫苗行业资讯周刊(67)
沃森生物:公司通过新冠mRNA疫苗的研发与合作方一起建立了mRNA疫苗技术平台
沃森生物23价肺炎疫苗正式供应菲律宾国家免疫计划
中印尼HPV疫苗合作,为印尼女性构筑健康屏障
康希诺:产品“吸附无细胞百(三组分)白破联合疫苗”取得注册证
5月1日起,疫苗行业刑事红线全面收紧!3个旧套路直接入刑
重磅获批!成大生物狂苗“简易4针法”免疫程序获批
华兰疫苗:流感病毒mRNA疫苗、新型佐剂流感疫苗正在开展临床前研究
万泰生物厦门子公司疫苗临床试验获批
沃森生物:公司和子公司自主研发的吸附破伤风疫苗目前已进入Ⅲ期临床试验阶段
康药业两款mRNA疫苗YKYY025、YKYY026获国家药品监督管理局临床试验批准
01#
官方信息
INDUSTRIAL DLOPMENT
沃森生物:公司通过新冠mRNA疫苗的研发与合作方一起建立了mRNA疫苗技术平台
沃森生物4月15日在投资者关系平台上答复投资者关心的问题。
投资者:mRNA 技术平台的建成对公司长期发展有什么战略意义?将如何改变公司的产品结构和盈利能力?
沃森生物董秘:从全球来看,mRNA 创新技术平台历经数十年技术沉淀,打破了传统疫苗研发模式的限制,过去几年,全球创新疫苗企业借助该技术已累计创造了较高的商业价值。经过多年的持续投入,中国创新疫苗企业也已建立了自己的 mRNA 疫苗技术平台,部分疫苗企业已在多款 mRNA 疫苗上有研发布局。mRNA 技术具有广泛的应用前景,与其它技术相比,其具有递送效率更高、开发周期短、生产成本低等显著优势。公司通过新冠 mRNA 疫苗的研发与合作方一起建立了 mRNA 疫苗技术平台,并在该平台上继续研发了呼吸道合胞病毒 mRNA 疫苗、冻干带状疱疹病毒 mRNA 疫苗等疫苗产品,进一步丰富了公司在研产品管线,若相关产品后续上市后还将有利于进一步增强公司的盈利能力,夯实公司核心竞争力。关于公司 mRNA 疫苗平台建设及相关产品的后续进展情况请持续关注公司的信息披露。公司郑重提醒投资者,疫苗产品的研发、临床研究、审评、审批的进度和结果等均具有一定的不确定性,敬请投资者注意投资风险。
沃森生物23价肺炎疫苗正式供应菲律宾国家免疫计划
4月14日,据沃森生物消息,近日,沃森生物控股子公司玉溪沃森生物技术有限公司开始正式向菲律宾卫生部交付23价肺炎球菌多糖疫苗(PPSV23),供应其2026年扩大免疫计划(EPI),标志着该疫苗首次成为免疫规划用苗。此前,公司已中标2025年菲律宾PPSV23国家采购项目,于2026年开始供应。
该产品是全球首支不含防腐剂的23价肺炎球菌多糖疫苗,适用于2周岁以上儿童及成人高危人群,目前全球累计销量已突破1400万剂。其安全性与有效性已获国内外临床研究的双重验证——国内与国外III期临床试验结果高度一致,均显示其免疫原性非劣于国际主流同类产品。目前,该疫苗已先后进入印度、科特迪瓦、乌兹别克斯坦、萨尔瓦多等市场,向孟加拉国供应产品原液,并在其他多国开展技术转移本地化生产合作,国际化布局持续深化。
康希诺:产品“吸附无细胞百(三组分)白破联合疫苗”取得注册证
每经AI快讯,康希诺4月12日晚间发布公告称,康希诺生物股份公司近日获得国家药品监督管理局下发的婴幼儿用吸附无细胞百(三组分)白破联合疫苗《药品注册证书》。产品名称为“吸附无细胞百(三组分)白破联合疫苗”。
批签发大幅下滑,HPV疫苗市场遇冷明显
我国HPV(人乳头瘤病毒疫苗)市场正经历显著调整。
21世纪经济报道记者根据中国食品药品检定研究院披露的数据初步统计,2026年第一季度(截至3月29日),HPV疫苗批签发次数为27批,其中玉溪泽润生物的二价HPV疫苗获批签发16批,万泰生物的九价HPV疫苗获批9批;这一数据与2025年一季度HPV疫苗共获批签发45批相比,出现大幅下降。
5月1日起,疫苗行业刑事红线全面收紧!3个旧套路直接入刑
最高法、最高检4月10日发布的《关于办理贪污贿赂刑事案件适用法律若干问题的解释(二)》(以下简称《解释(二)》),5月1日起施行后,将直接推翻疫苗行业多年的“灰色避险逻辑”,行业曾经依赖的“三板斧”彻底失效,违规风险陡增。
重磅获批!成大生物狂苗“简易4针法”免疫程序获批
成大生物4月17日公告,公司收到国家药监局核准签发的药品补充申请批准通知书,公司就冻干人用狂犬病疫苗(Vero细胞)提出的补充申请,在该疫苗现有免疫程序基础上,增加简易4针(简称“简易4针法”)免疫程序,并同步修订说明书和标签内容,已经正式获得批准。
02#
文献解读
INDUSTRIAL DLOPMENT
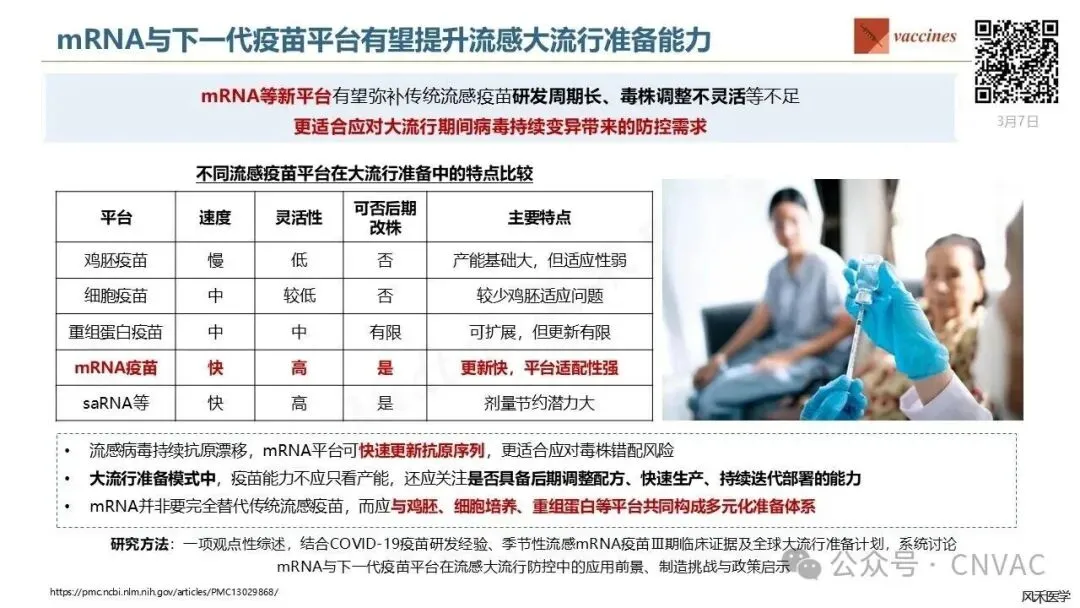
mRNA与下一代疫苗平台有望提升流感大流行准备能力
03#
国际新闻
INDUSTRIAL DLOPMENT
中印尼HPV疫苗合作,为印尼女性构筑健康屏障
“HPV(人乳头瘤病毒)疫苗对印度尼西亚女性很重要,因为它能保护我们免受宫颈癌的侵害。”印尼女子伊塔坚定地对新华社记者说。然而,HPV疫苗价格高昂且供应不足的现实依然横亘在许多家庭面前。“如果疫苗能够实现本土化生产、价格更亲民,我们作为家长不仅更易获得,也更愿意推荐给他人。”身为母亲的伊塔说。
伊塔的心声折射出印尼普通家庭的关切。在成本高、供给紧与分配不均等多重挑战下,HPV疫苗可及性的提升正成为印尼公共卫生体系的重要课题。
印尼食品与药品管理局局长塔鲁纳·伊克拉尔近日接受新华社记者专访时说,印尼正不断深化与中国在疫苗领域的合作,以扩大HPV疫苗覆盖面,并加快本土研发与生产能力建设。
他介绍说,印尼拥有近3亿人口,分布在1.7万多座岛屿上,复杂的地理条件使医疗资源配送长期面临挑战。面对宫颈癌这一严峻的公共卫生问题,推广预防有效率超过90%的九价HPV疫苗尤为关键。“预防是公共卫生体系中最重要的一环,而疫苗接种则是最具成本效益的防线”。
在他看来,与中国在生物制药领域的合作,给印尼带来了“战略性跃升”——这种合作不仅是技术引进,更是能力共建,让印尼得以在较短时间内对接国际先进标准,加快从“依赖进口”向“自主制造”的转变。“与中国伙伴的协作,使印尼能够跨越早期摸索阶段,直接进入高水平发展轨道。”他说。
伊克拉尔回忆起此前赴中国北京、上海、深圳等地考察的经历时表示,实地调研让他更加坚定推动合作的决心。他期待双方未来能构建起涵盖政府对话、产业协同与科研合作的多层次合作体系,形成更具韧性的公共卫生合作网络。
他说,这种合作不仅关乎一国发展,也体现了亚太地区国家之间在公共卫生领域的互助与共赢。“合作胜于竞争,在相互信任的基础上,我们能够共同提升应对健康挑战的能力。”
印尼本土生物制药企业正成为相关合作的重要承接者。印尼埃塔纳生物技术公司生产主管维诺表示,与中国开展技术合作,是推动疫苗本土化生产的关键一步。“通过建立完善的质量体系,并与中国伙伴保持密切协作,我们确保疫苗能够达到国际标准。”
维诺预计,在实现全面本土化生产后,印尼每年可生产数百万剂HPV疫苗,在稳定供应的同时显著降低接种成本,为更多女性筑起抵御宫颈癌的健康防线。
业内人士认为,这种以技术共享和产能合作为基础的模式,不仅有助于提升单一国家的公共卫生能力,也为区域疫苗供应链的稳定提供了新的支撑。
对像伊塔这样的家庭而言,这一进程意味着切实可感的变化。她的女儿阿莱娜已在学校完成HPV疫苗接种。伊塔说,“如果获取更方便,我相信会有更多父母愿意为孩子迈出这一步”。
04#
最新临床/批签发
INDUSTRIAL DLOPMENT
万泰生物厦门子公司疫苗临床试验获批
近日,万泰生物发布公告,其全资子公司厦门万泰沧海生物技术有限公司收到国家药监局核准签发的药物临床试验批准通知书,公司申报的“重组呼吸道合胞病毒疫苗(CHO细胞)”临床试验申请获批,同意开展用于预防由呼吸道合胞病毒(RSV)感染引起的下呼吸道疾病的临床试验。
该疫苗由厦门大学与厦门万泰沧海生物技术有限公司联合研制,采用基因工程重组技术研发,主要活性成分为企业自主开发的RSV融合前构象膜融合蛋白F,是福建生物医药产业创新研发的重要成果。此次临床试验获批,标志着这款重组呼吸道合胞病毒疫苗正式进入临床研究阶段,将为后续疫苗上市、满足公众预防RSV感染相关疾病需求奠定坚实基础。
沃森生物:公司和子公司自主研发的吸附破伤风疫苗目前已进入Ⅲ期临床试验阶段
每经AI快讯,有投资者在投资者互动平台提问:吸附破伤风疫苗已挺进III期临床,这款产品将如何完善公司成人疫苗矩阵,为业绩带来新的增长点?
沃森生物4月15日在投资者互动平台表示,公司和子公司玉溪沃森生物技术有限公司自主研发的吸附破伤风疫苗已完成了Ⅰ期临床试验阶段现场主要研究工作,目前已进入Ⅲ期临床试验阶段。本疫苗主要用于发生创伤机会较多的人群,接种本疫苗后,可刺激机体产生体液免疫应答,用于预防破伤风。公司将按照国家药品注册临床试验的有关规定,积极推进该疫苗的Ⅲ期临床试验工作。本疫苗在完成Ⅲ期临床试验,且研究结果达到临床试验方案规定的评价标准后,方能组织开展申请上市许可的相关工作。Ⅲ期临床试验的时间和结果均具有一定的不确定性,后续对于临床试验、申请上市许可等的进展情况,公司将按照相关法规和规范性文件的规定及时履行信息披露义务。请持续关注。
康药业两款mRNA疫苗YKYY025、YKYY026获国家药品监督管理局临床试验批准
近日,悦康药业集团股份有限公司子公司北京悦康科创医药科技股份有限公司、杭州天龙药业有限公司获得国家药品监督管理局(NMPA)核准签发的《药物临床试验批准通知书》,旗下两款自主研发 mRNA 疫苗——YKYY025 注射液(用于预防呼吸道合胞病毒(RSV)引起的下呼吸道疾病)、YKYY026 注射液(用于预防带状疱疹)均获批开展临床试验。据悉,这两款创新疫苗此前已成功获得美国食品药品监督管理局(FDA)临床试验批准,实现中美双报双批。
华兰疫苗:流感病毒mRNA疫苗、新型佐剂流感疫苗正在开展临床前研究
4月9日,华兰疫苗在互动平台回答投资者提问时表示,公司流感病毒mRNA疫苗、新型佐剂流感疫苗正在开展临床前研究,未来若达到信息披露标准,公司将对相关信息进行披露。
征稿
“E苗工坊”长期面向预防接种医生、医药代表和有关疫苗、疾病预防、防疫行业、疫苗营销领域的专业人员征稿,稿费不等(或文章内容与以上行业相关),高质量稿件还会获得惊喜礼品一份,有意者请与公众号运营人员联系,期待大家的投稿!
QQ邮箱:845597821@qq.com
好内容请转发,让更多精进成长的人获益。

