科学妥协于营销:用37年证明1款防癌疫苗
疫苗学的最终目的,是实现消除性免疫——即在病原进入机体时消除病原体,避免症状的出现。研究显示,预防50%的感染所需的抗体水平,远远超过预防50%的重症发生。然而现实很割裂:在宣传上疫苗预防的疾病越严重,这款疫苗就越畅销。可能源于公众潜意识将疫苗理解成一种兼具预防+治疗作用的东西。
上世纪80年代,由于默克公司的乙肝疫苗未能将预防肝癌写入说明书适应症,且仅被CDC推荐用于职业暴露的高危人群接种导致销量不佳。最终结合人道主义原则,以数百万美元将专利技术出让给了中国。
此后默克公司吸取教训,积极与FDA沟通将宫颈癌写入适应症,最终也得偿所愿。当前GSK也在积极开展RCT临床试验,争取能够将预防老年痴呆写入适应症。此外,国外对流感疫苗的适应症也在积极进行新的探索,越来越多的新证据已经指向对心血管疾病等并发症的预防作用。
尽管HPV疫苗是全球首个将癌症写进说明书适应症的疫苗,但学界普遍认为它并不是唯一、也不是第一个能够防癌的疫苗。乙肝疫苗也被学界普遍认为是预防肝癌的有效手段,但由于缺乏直接针对肝癌这一临床终点的RCT临床试验结果或高质量的真实世界研究证据,导致说明书适应症并非肝癌而是肝炎。从HBV感染到肝癌,通常需要20年以上的时间。如果以肝癌作为临床试验终点,那么疫苗就无法上市。
2022年,国家癌症中心在肿瘤学顶刊Cancer Letters(IF:10.1)发表了一项研究,通过长达37年的随访和随机对照研究的形式,将乙肝疫苗能够预防肝癌这一结论从理论变成现实。尽管已经错过了将预防肝癌写进说明书适应症的机会,但高危人群仍然有必要将乙肝疫苗接种提升日程。
这项研究在曾经的全国有名的肝癌高发区江苏省启东市开展,研究从1983年开始,截止到2020年一共历时37年。研究为整群随机对照试验,按照1:1比例共纳入8万多名新生儿。
结果显示:5岁组、10岁组和成年期的疫苗组HBsAg携带率均显著低于对照组(对照组),以成年组为例,疫苗组HBsAg携带率为2.02%,对照组为8.11%。最重磅的是对肝癌的预防效果:
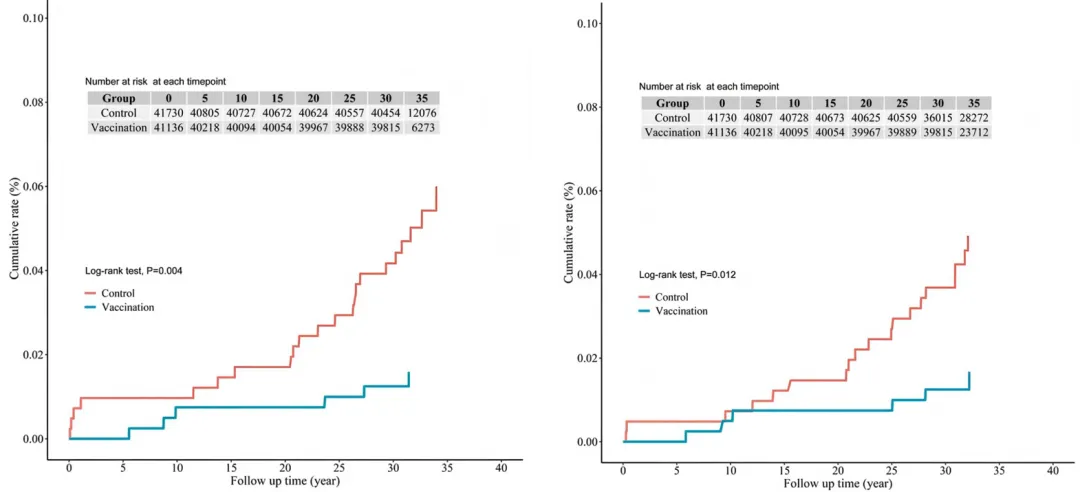
疫苗组的肝癌发病率为0.46/10万例,对照组为1.61/10万例,疫苗对预防肝癌发生的保护效力为72% (95% CI: 30%–89%),对因肝癌死亡的保护效力为70%(95% CI: 23%–88%)。
图左:疫苗组和对照组的肝癌发病率;图右:疫苗组合对照组的肝癌死亡率。
如果结合肝癌归因比来看,乙肝疫苗预防肝癌的保护效力还要更高。在可检测HBV状态的肝癌病例中,75%的病例与HBV感染相关,HBV阳性者的肝癌发病率(12.33/10万人年)远高于阴性者(0.21/10万人年)。若仅以归因于HBV的肝癌推算,则乙肝疫苗预防HBV所致肝癌的有效性可超过90%。(黄曲霉毒素、酒精等也能导致肝癌)
尽管得到了想要的结果,但从结果上仍然可以看到试验验证的困难性:肝癌作为我国发病率TOP的恶性肿瘤,在8万人的样本量和37年的随访下,最后也仅得到28例肝癌终点病例(疫苗组6例,对照组22例)。因此,若企业在开发乙肝疫苗时想要将预防肝癌写入适应症,需要付出的代价不可计数。
启东市的这项研究,其实可以算是对我国台湾地区另外一项大型长期随访队列研究的结果科学复现。早在1997年,《新英格兰医学杂志》就发表了全民乙肝疫苗接种计划后的少年儿童的肝癌发病率随访研究结果。结果显示:6~14岁儿童的肝癌发病率从1981~1986年的0.7例/10万人,下降至1990~1994年的0.36例/10万人。
到2009年时这项研究已经跨越了20年,最终显示乙肝疫苗对6~19岁青少年的肝癌保护率达到69%(p<0.001),研究被发表在《国家癌症研究所杂志》上。
HBV感染到症状性肝炎的出现,仅需要经过几十天的潜伏期即可实现。如果以预防肝炎作为预防肝癌的临床替代终点,那么乙肝疫苗临床试验的周期将大大缩短。并且以症状性肝炎为临床试验终点,比以肝癌作为临床试验终点更具可行性。
后来在将乙肝疫苗纳入免疫规划、人群已经建立起针对HBV的免疫水平后,新研发的乙肝疫苗再以肝炎作为临床试验终点也已经不具有可行性,以肝癌为临床终点更不可行也不人道。此后学界建立了乙肝表面抗体和保护率之间的关联,则又进一步采用了抗体水平来代替乙肝疫苗预防肝炎的效果,无需再通过事件驱动验证完成适应症的批准。
HPV疫苗也面临着相似的问题,为了避免此类情况发生,默克公司在研发HPV疫苗时就向FDA争取过将预防癌症写入说明书。但面临的问题和乙肝疫苗一样严峻——从HPV感染到宫颈癌平均需要15~20年。要知道目前第一款HPV疫苗上市至今也不过20年,如果以宫颈癌为研发临床终点,那么这款疫苗要至少推迟10年才能上市。
最初医学界发现——对CIN2/3(2级或3级宫颈上皮内病变)治疗后可有效降低宫颈癌的发生,猜测CIN2/3是宫颈癌的前驱症状。因此在FDA的许可下,最初的HPV疫苗研发采用了以CIN2/3为临床替代终点的方式评估疫苗预防宫颈癌的效果。理论闭环为:疫苗能够有效预防CIN2/3的发生,那么也就能够预防宫颈癌的发生。
尽管当时学界已经通过解剖学和归因方法学确认了HPV感染是宫颈癌的必要条件和原因,但临床试验仍采取了保守策略——宫颈癌是HPV感染所致的结论是从后往前推得到的(99.7%的宫颈癌病例检测到HPV感染),而非从前向后推论(感染HPV最终会得宫颈癌,没感染HPV者没有得宫颈癌),临床试验也是从前向后推(打的疫苗人没有发生宫颈癌,没打疫苗者发生了宫颈癌)。
为了以防万一,因此当时仍然以CIN2/3为临床试验替代终点(即使上述因果关系是假的、疫苗是无效的,也能够在自然进展为CIN2/3时及时进行发现治疗不至于发展为宫颈癌)。
但分析保护率时,前提一定是:确诊的CIN2/3患者需要检出对应型别的HPV感染才能归因于HPV疫苗的预防作用,否则即使预防了CIN2/3也不能归结于疫苗作用。这由HPV疫苗的原理决定:HPV疫苗通过特异性中和抗体发挥对HPV病毒的预防作用,最终导致了CIN2/3这一由HPV感染所致结局的发生,否则疫苗效力难以解释。
此后,许多大型前瞻性研究开始介入进来:如果通过从前往后推的方式验证,HPV感染者最终是否会得宫颈癌?结果确实如理论推测的那样:初始HPV阳性者,会经历转阴和维持状态(高危型HPV持续感染)。超过12个月后,一部分开始转阴或仍然维持持续阳性状态,而剩余部分则开始进展为CIN2/3。
再后来随着HPV DNA检测方法作为主要筛查手段被引入,医学界发现,通过早期识别HPV持续感染(初始高危型HPV阳性后间隔1年后复测阳性,转诊阴道镜)几乎能够提前识别所有的CIN2/3患者,这与通过对CIN2/3进行治疗来预防宫颈癌的原理基本一致。
随着WHO和美国国家癌症中心将预防HPV持续感染作为评价HPV疫苗效力的主要终点,至此HPV预防宫颈癌的逻辑链条真正清晰起来:HPV疫苗通过预防HPV持续感染发挥作用,预防了HPV持续感染,相应的癌症就不会发生。这也与乙肝疫苗通过预防乙型肝炎的方式,实现预防肝癌的目的高度相似。
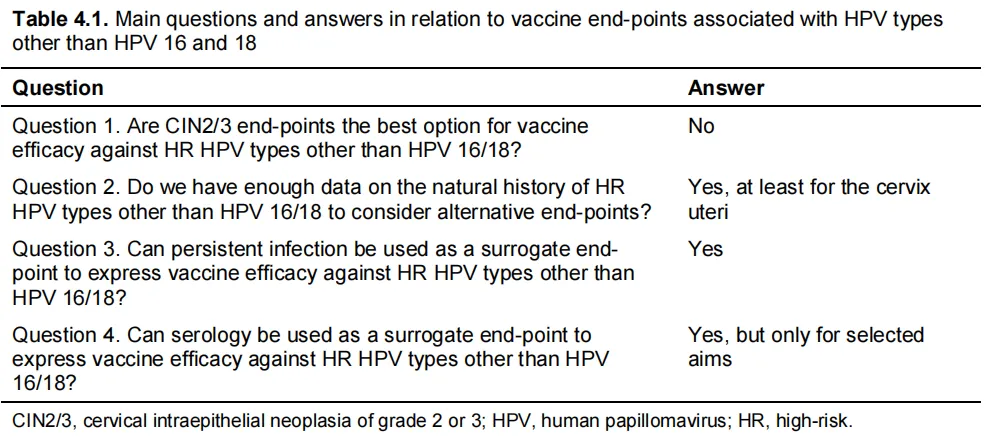
国际癌症研究机构及美国国家癌症中心:表4.1 与HPV16和18以外的HPV型别相关的疫苗终点的主要问题和答案。
直到十几年后的2020~2021年,《新英格兰医学》和《柳叶刀》杂志才相继发布了针对宫颈癌这一临床结局的真实世界有效性数据,确认HPV疫苗可以通过预防HPV感染来降低宫颈癌的发生率。然而在此之前,HPV疫苗已经作为防癌疫苗被宣传了很多年。
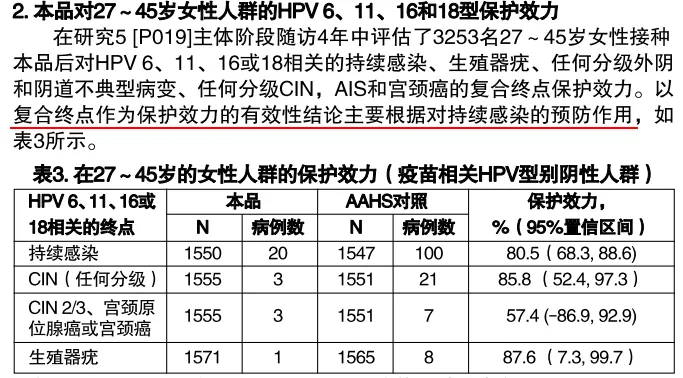
期间更多的HPV疫苗也参与到了使用新共识推荐的临床试验替代终点中来:四价HPV疫苗(酿酒酵母)在扩龄至27~45岁时,其针对CIN2/3临床终点的保护效力试验无统计学意义,最终使用持续感染数据获批扩龄。
GSK的二价HPV疫苗也面临着相同的情况,说明书中明确写到“目前尚未证实本品在26岁及以上女性中预防HPV16和18相关的CIN 2/3、AIS 或宫颈癌的保护效力。”即获批26~45岁女性预防宫颈癌的适应症,也是基于预防持续感染的推测。
九价HPV疫苗(酿酒酵母)甚至越过WHO的主要推荐,使用尚未与保护率建立起关联的免疫原性数据推测预防持续感染和病变的效力,将疫苗适用人群扩龄至27~45岁时。而为了进一步强调疫苗对其他癌症的预防作用以扩大销售,FDA基于对疫苗对宫颈部位持续感染的作用提前批准了疫苗能够预防口咽癌这一适应症——在美国,口咽癌的新发病例数超过宫颈癌。
目前带状疱疹疫苗同样遇到这样的困境——在仅宣传与带状疱疹有关的适应症时,接种率始终难以快速上升。而这两年最为人知的宣传则是带疱疫苗有预防“老年痴呆”的功效,但当前大多数研究并非RCT试验。为此,重组带状疱疹疫苗的生产企业GSK已经宣布将启动针对老年痴呆预防效果的RCT试验,未来有望获批预防老年痴呆这一适应症。
Wahl I, Wardemann H. Sterilizing immunity: Understanding COVID-19. Immunity. 2022 Dec 13;55(12):2231-2235.
Khoury DS, Cromer D, Reynaldi A, et al. Neutralizing antibody levels are highly predictive of immune protection from symptomatic SARS-CoV-2 infection. Nat Med. 2021 Jul;27(7):1205-1211Cao M, Fan J, Lu L, et al. Long term outcome of prevention of liver cancer by hepatitis B vaccine: Results from an RCT with 37 years. Cancer Lett. 2022 Jun 28;536:215652.
Chang MH, Chen CJ, Lai MS, et al. Universal hepatitis B vaccination in Taiwan and the incidence of hepatocellular carcinoma in children. Taiwan Childhood Hepatoma Study Group. N Engl J Med. 1997 Jun 26;336(26):1855-9.
Chang MH, You SL, Chen CJ, et al. Decreased incidence of hepatocellular carcinoma in hepatitis B vaccinees: a 20-year follow-up study. J Natl Cancer Inst. 2009 Oct 7;101(19):1348-55.
Lei J, Ploner A, Elfström KM, et al. HPV Vaccination and the Risk of Invasive Cervical Cancer. N Engl J Med. 2020 Oct 1;383(14):1340-1348.
Falcaro M, Castañon A, Ndlela B, et al. The effects of the national HPV vaccination programme in England, UK, on cervical cancer and grade 3 cervical intraepithelial neoplasia incidence: a register-based observational study. Lancet. 2021 Dec 4;398(10316):2084-2092.
IARC HPV Working Group. Primary End-points for Prophylactic HPV Vaccine Trials. Lyon (FR): International Agency for Research on Cancer; 2014. PMID: 26468561 四价/九价人乳头瘤病毒疫苗(酿酒酵母)说明书.
双价人乳头瘤病毒吸附疫苗说明书.



评论